Présentées au congrès annuel SGO (Society of Gynecologic Oncology) et publiées dans le même temps dans le New England Journal of Medicine, les (très attendues) études RUBY et NRG GY018 transforment le paysage thérapeutique dans les cancers de l’endomètre avancés.
Pour rappel : la chimiothérapie par Carboplatine Paclitaxel est le standard de 1ere ligne des cancers de l’endomètre métastatiques.
L’immunothérapie se positionne actuellement en 2e ligne après platine : seule avec le dostarlimab (étude GARNET, tumeurs dMMR, indication non remboursée en France) ou dans l’association Lenvatinib Pembrolizumab (étude KEYNOTE 775, indépendamment du profil MMR, disponible en accès précoce).
A l’image du cancer bronchique, une association chimiothérapie + immunothérapie a-t-elle une place en 1ère ligne ?
C’est la question posée par ces 2 études :
L’étude RUBY est une étude de phase III qui randomisait Carboplatine Paclitaxel versus Carboplatine Paclitaxel + Dostarlimab (6 cycles puis maintenance jusqu’à 3 ans)
Au total : 494 patientes, cancers de l’endomètre avancés stade III-IV avec maladie mesurable
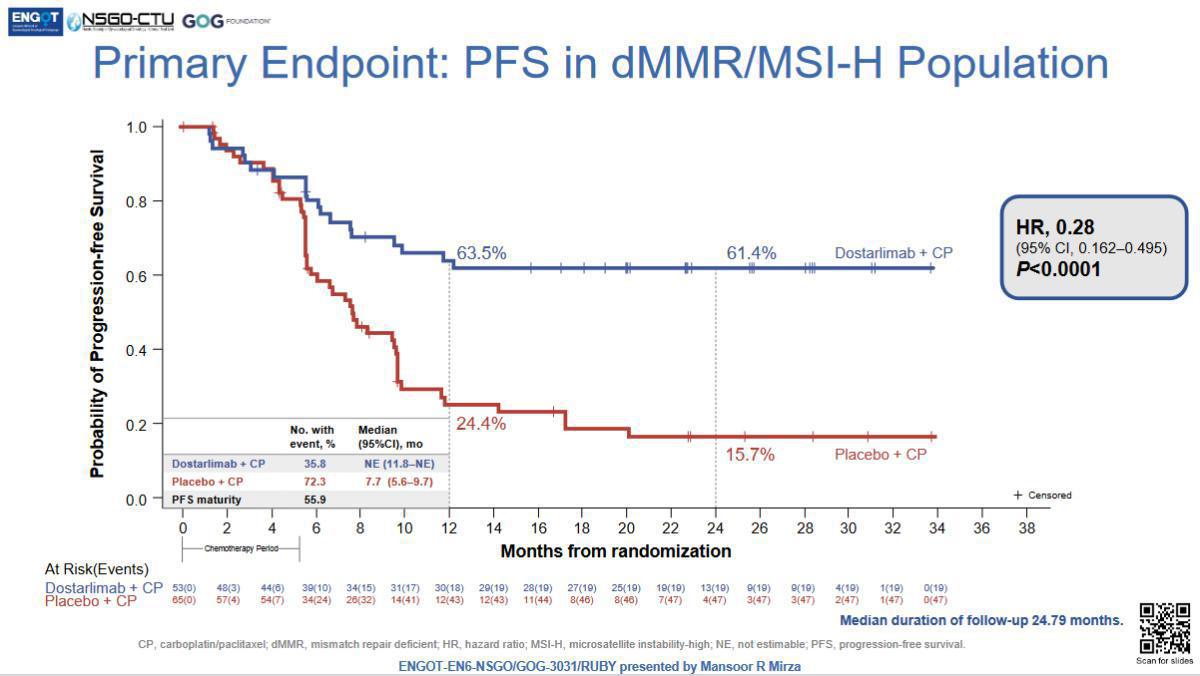
Analyse dans la population dMMR/MSI high (23.9% de la population)
- PFS à 24 mois = 61.4% (CT-dostarlimab) versus 15.7% (CT-placebo) : HR = 0.28, p<0.001
- OS à 24 mois = 83.3% (CT-dostarlimab) versus 58.7% (CT-placebo) : HR = 0.30
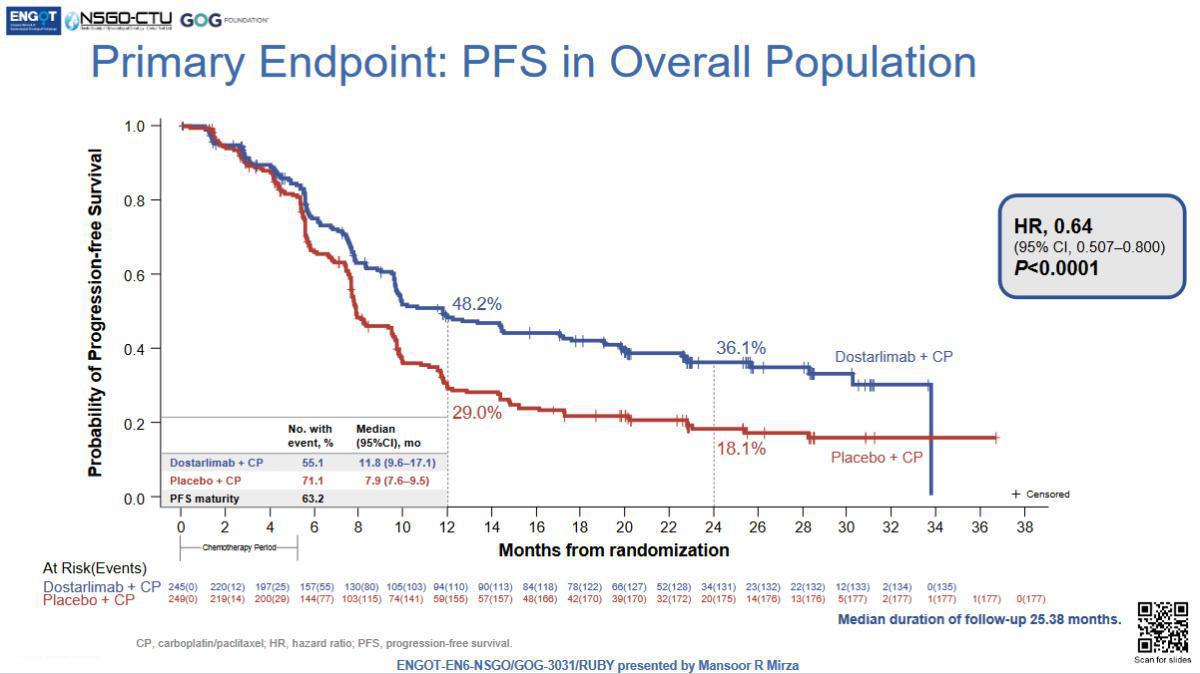
Analyse dans la population globale
- PFS à 24 mois = 36.1% (CT-dostarlimab) versus 18.1% (CT-placebo) : HR = 0.64, p<0.001
- OS à 24mois = 71.3% (CT-dostarlimab) versus 56% (CT-placebo) : HR = 0.64, p = 0.0021
Le profil de toxicité est acceptable sans nouveau signal de toxicité avec l’association chimiothérapie + immunothérapie ni dégradation de la qualité de vie.
L’étude NRG GY018 est une étude de phase III qui randomisait Carboplatine Paclitaxel versus Carboplatine Paclitaxel + Pembrolizumab (6 cycles puis maintenance jusqu’à 14 cycles)
Au total : 816 patientes, cancers de l’endomètre avancés stade III-IV avec maladie mesurable
591 pMMR / 225 dMMR
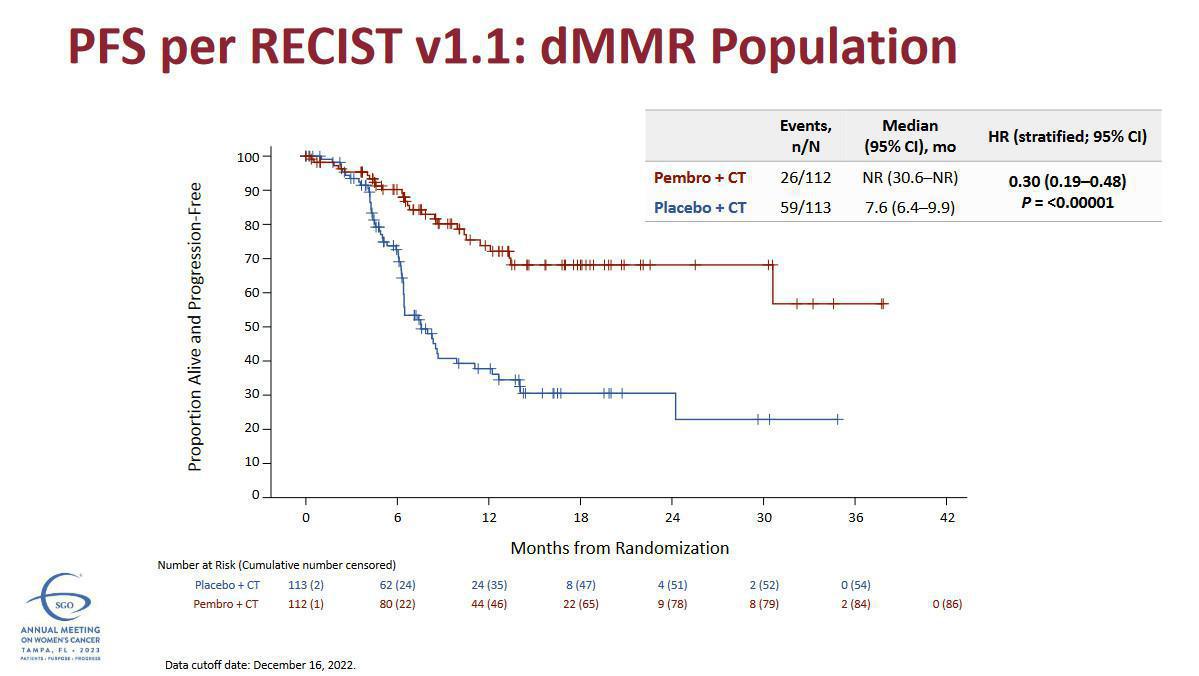
Analyse dans la population dMMR/MSI high (27.6% de la population)
- PFS à 12 mois = 74% (CT-pembrolizumab) versus 38% (CT-placebo) : HR = 0.30 p<0.001
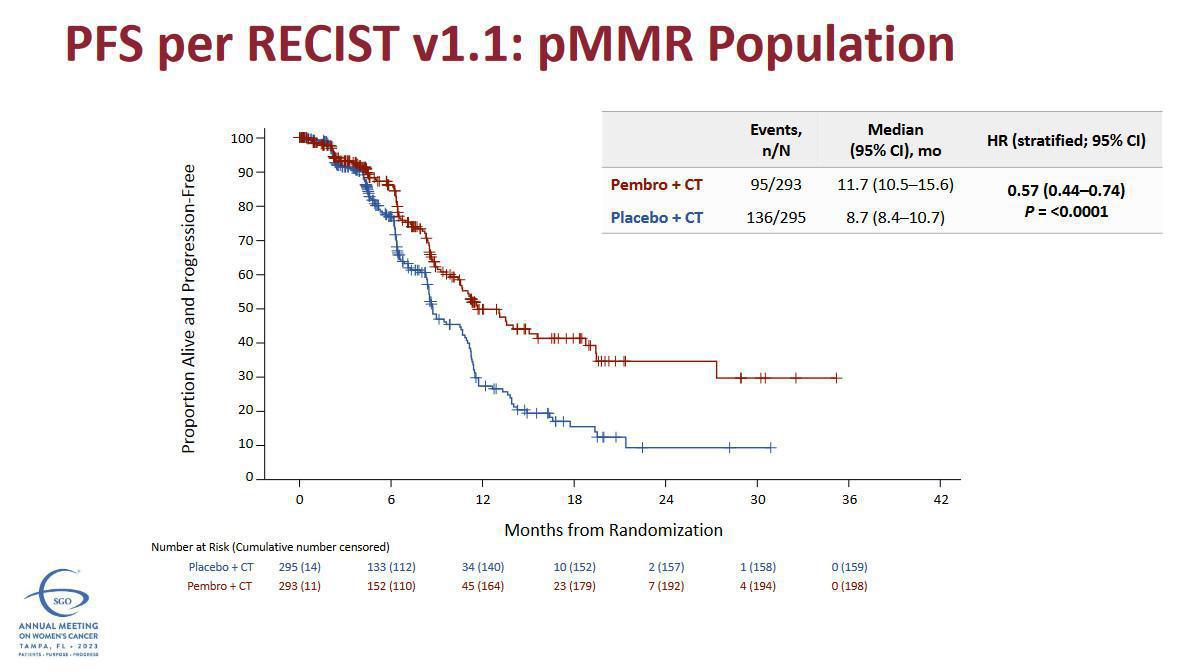
Analyse dans la population pMMR/MSS
- Median PFS = 13.1 mois (CT-pembrolizumab) versus 8.7 mois (CT-placebo) : HR = 0.54 p<0.001
Le profil de toxicité est acceptable sans nouveau signal de toxicité avec l’association chimiothérapie + immunothérapie ni dégradation de la qualité de vie.
En pratique : Après 10 ans avec le même standard « Carboplatine Paclitaxel », 2 études de phase III publiées simultanément dans le NEJM (rien que ca !) viennent bousculer les codes en 1ère ligne des cancers de l’endomètre avancés :
Nous retiendrons de ces 2 études :
- Bénéfice en PFS de l’association Carboplatine Paclitaxel + anti-PD1 par rapport à Carboplatine Paclitaxel
- Ce bénéfice est majeur et sans précédent dans la population dMMR/MSI high (25% des cancers de l’endomètre métastatiques) avec un Hazard Ratio à 0.30 (!!!) soit une diminution du risque de progression de 70%.
- Un bénéfice également dans la population pMMR (effet immunogène de la chimiothérapie probable).
- La survie globale dans l’étude RUBY manque de maturité (33%) mais semble montrer une tendance d’amélioration avec l’ajout du dostarlimab.
- Le profil de tolérance de l’ajout d’un anti-PD1 à la chimiothérapie est satisfaisant avec des toxicités attendues en accord avec les différentes molécules.
Chimiothérapie + anti-PD1 va donc devenir notre nouveau standard de 1ère ligne pour les cancers de l’endomètre avancés
La prochaine étape ?
Immunothérapie seule pour les tumeurs dMMR ? C’est la question posée par l’étude DOMENICA (GINECO lead, Cocorico !) :
- Pour les cancers de l’endomètre dMMR/MSI en 1ère ligne : Dostarlimab versus Carboplatine Paclitaxel
- L’étude est ouverte aux inclusions : Tous les détails disponibles sur ACTIS Oncology
Editeur : Medicotech, 38 rue Leon, 75018 Paris
Directeur de la publication : Jean-David Fumet
Comité éditorial : François Ghiringhelli, Sylvain Ladoire, Didier Mayeur, Alice Hervieu, Benjamin Auberger, Benoite Mery, Christophe Sajous, Lauriane Eberst, Coriolan Lebreton, Sara Djemouai