Ces dernières années, la prise en charge thérapeutique du cancer du rein a connu une évolution majeure. La découverte des inhibiteurs de checkpoints immunitaires (anti-PD1/anti-PDL1 et anti-CTLA-4) a complètement révolutionné le paysage du carcinome rénal à cellules claires. L’immunothérapie d’abord utilisée en situation de 2ème ou 3ème ligne thérapeutique, est désormais présente dans tous les traitements standards de 1ère ligne métastatique sous la forme d’un doublet d’immunothérapie ou en association avec un inhibiteur de tyrosine kinase.
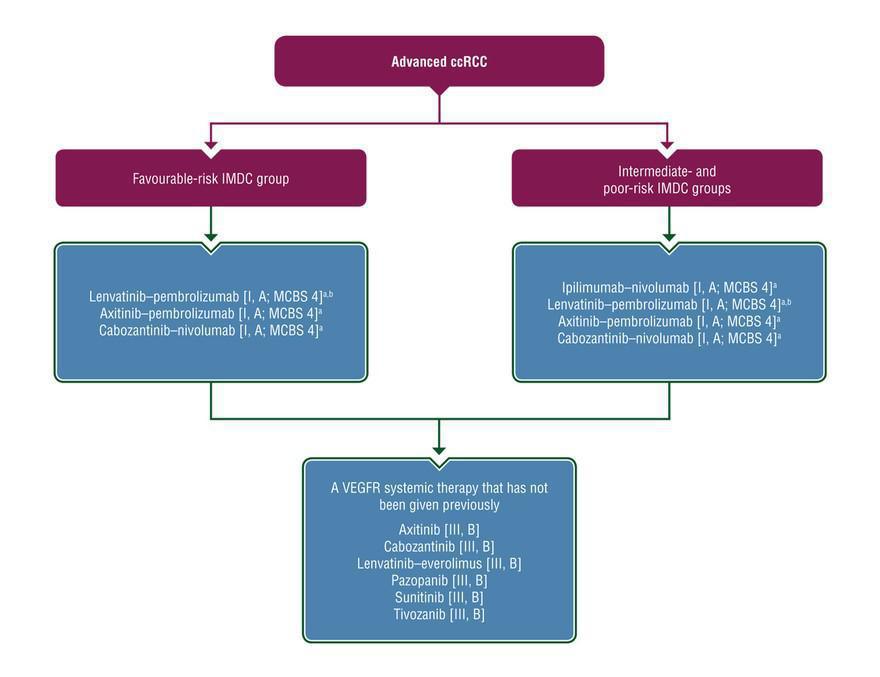
Les recommandations de l’ESMO ont récemment été mises à jour, suite aux données actualisées de plusieurs études de phase 3 qui évaluaient ces différentes combinaisons. Le choix du prescripteur est désormais guidé de manière consensuelle par les critères clinico-biologiques de l’IMDC qui définissent le pronostic des patients atteints de carcinome rénal métastatique en 3 catégories (pronostic favorable/intermédiaire ou défavorable).
En France, 3 associations sont désormais remboursées et validées en pratique courante :
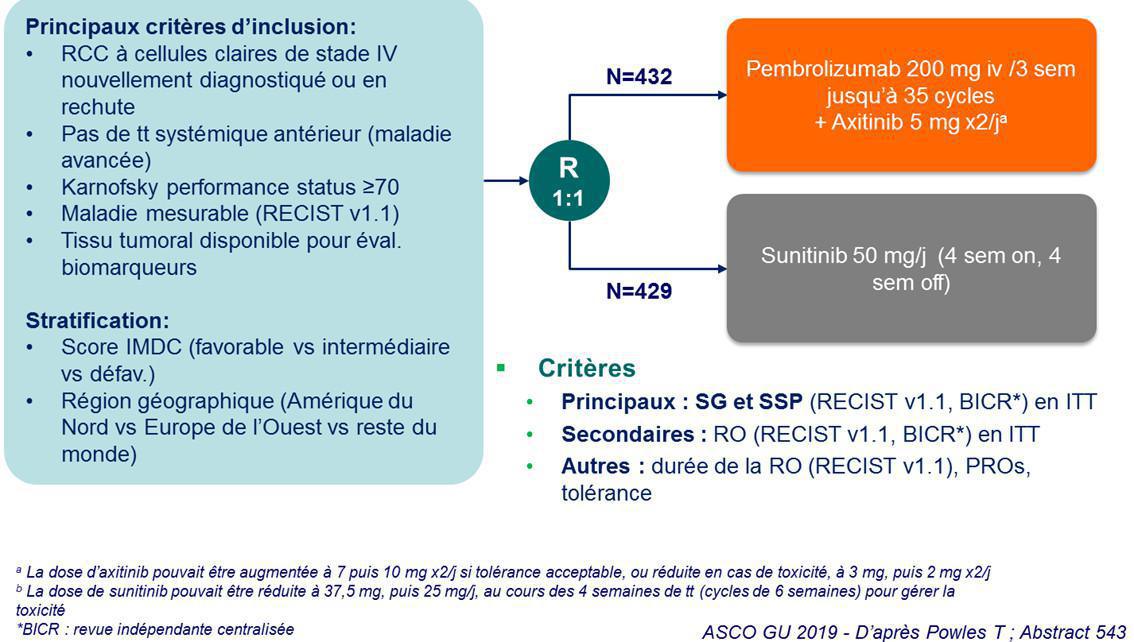
-Pembrolizumab associé à l’Axitinib (Etude KEYNOTE 426)
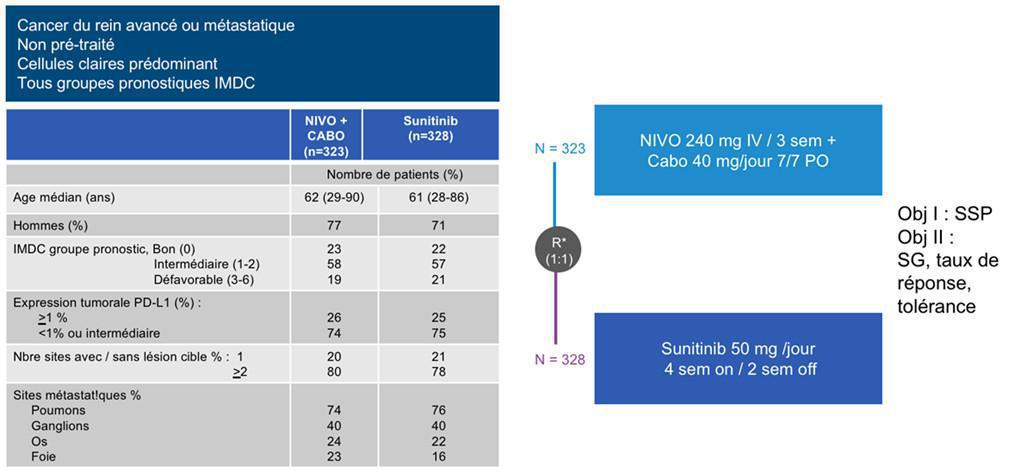
-Nivolumab associé au Cabozantib (Etude CHECKMATE-9ER)
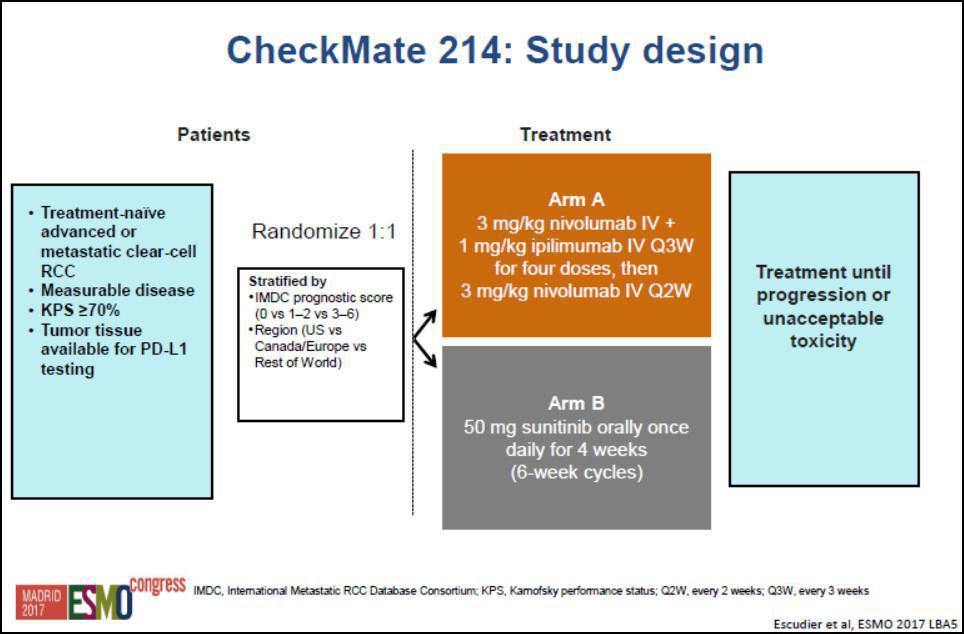
-Nivolumab associé à l’Ipilimumab (Etude CHECKMATE-214)
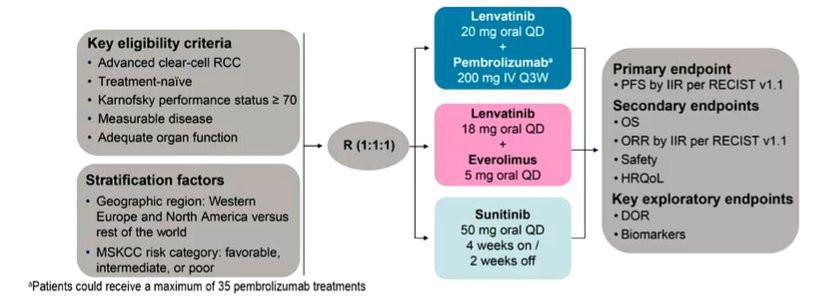
Les 2 premières combinaisons peuvent être utilisées chez l’ensemble des patients, indépendamment des critères de Heng et la dernière uniquement pour les patients atteints d'un carcinome à cellules claires métastatique de pronostic intermédiaire ou défavorable. Une 4ème association par Pembrolizumab et Lenvatinib, actuellement non remboursée, viendra probablement enrichir l’arsenal thérapeutique de nos malades dans les prochains mois, suite aux résultats de l’étude CLEAR dont les données actualisées après 33 mois de suivi médian ont été présentées lors du dernier congrès de l'ESMO - European Society for Medical Oncology
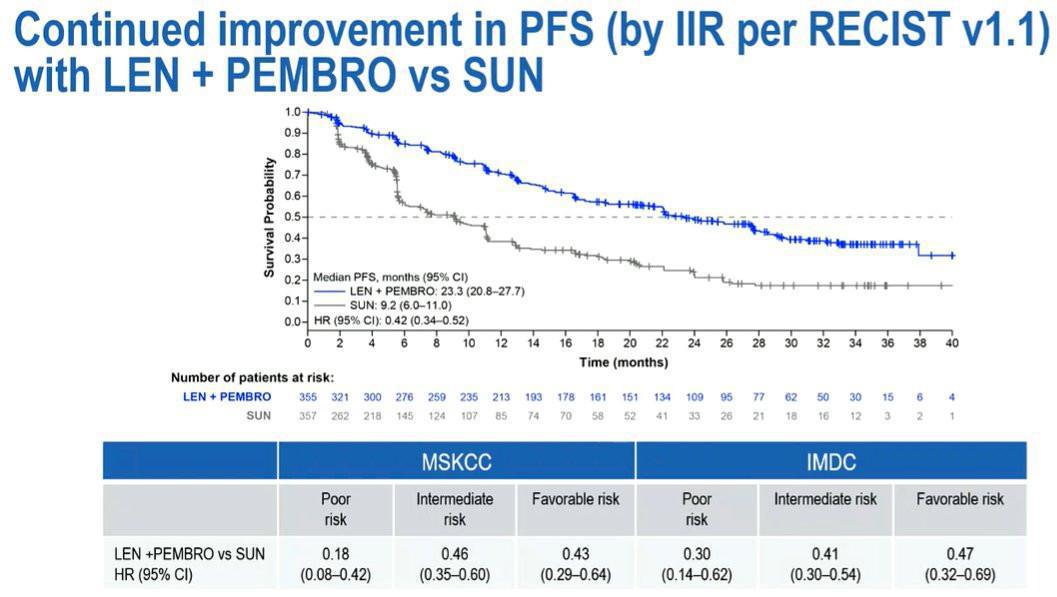
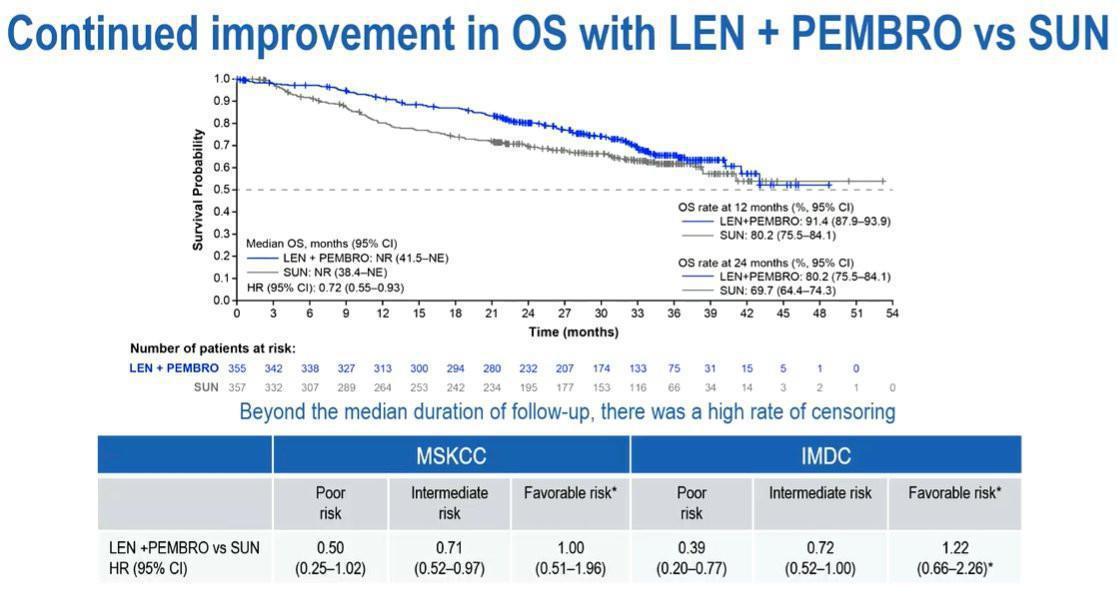
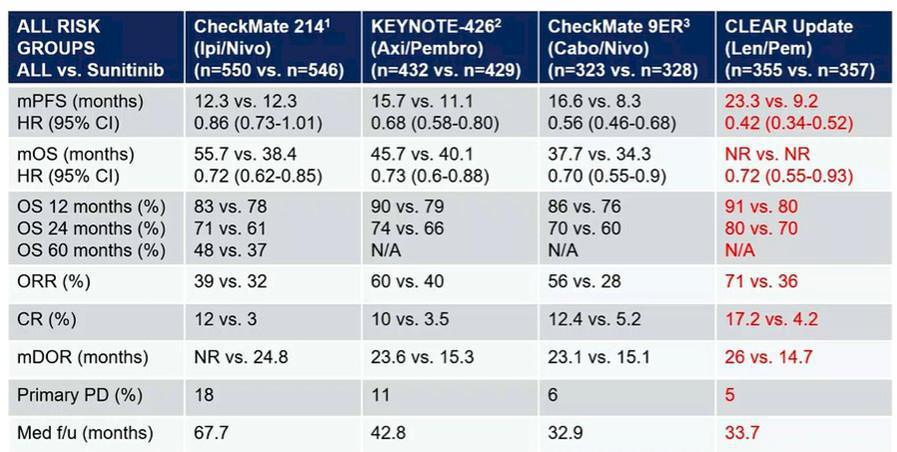
Cette étude confirmait un bénéfice significatif en survie sans progression pour tous les groupes pronostiques IMDC (23,3 mois pour l’association versus 9,2 mois pour le Sunitinib ; HR= 0,42 ; IC95% 0,34-0,52 ; p<0,0001). Concernant la survie globale, les données restent encore immatures en raison d’un nombre d’événements insuffisant même si le bénéfice semble s’observer uniquement pour les patients de pronostic intermédiaire ou défavorable. Le taux de réponse objective de 71% (dont 17,2% de réponse complète !) et la durée médiane de réponse de 26 mois font de cette association, une stratégie thérapeutique pertinente chez les patients avec une maladie symptomatique, pour peu qu’ils puissent la tolérer sur le long terme.
Si aucune comparaison directe n’est possible entre ces différentes combinaisons, qui avaient toutes comme bras comparateur un traitement par anti-angiogénique, l’étude des différents objectifs principaux ou secondaires et les analyses en sous-groupe restent instructives pour guider le prescripteur dans son choix thérapeutique.
D’autres éléments comme l’expérience du clinicien, le profil de tolérance de l’association et les facteurs liés à la maladie (sites métastatiques, caractéristiques histologiques, profil évolutif) et à ceux du patient, doivent également être pris en considération :
- Chez les patients avec une forte charge tumorale et une présentation clinique très bruyante au diagnostic, il sera proposé idéalement une combinaison par immunothérapie et ITK afin d’obtenir une réponse rapide
- Chez les patients ayant des localisations cérébrales (malades sous-représentés dans les essais thérapeutiques), plusieurs données (CABRAMET) ont montré une certaine efficacité en faveur du Cabozantinib, suggérant un passage satisfaisant de la barrière hémato-encéphalique. Le tropisme osseux également favorable pour cet inhibiteur de tyrosine kinase, plaide également pour une utilisation de l’association par Nivolumab et Cabozantinib chez ces malades.
- Chez les patients atteints d’un carcinome rénal avec contingent sarcomatoïde, les données post-hoc de l’étude CHECKMATE-214 font état d’un taux de réponse impressionnant de 61% (dont 19% de réponse complète) faisant de la combinaison Nivolumab et Ipilimumab le traitement de choix concernant cette population.
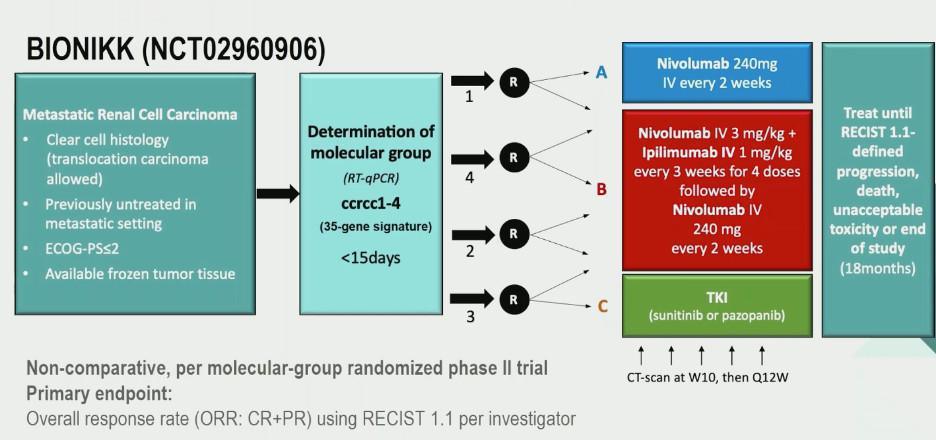
L’étude de phase 2 BIONIKK, récemment publié dans The Lancet Oncology, a suggéré que la réponse au traitement par Nivolumab, Nivolumab associé à l’Ipilimumab ou par inhibiteurs de tyrosine kinase pouvait varier en fonction du microenvironnement tumoral. Elle est la première à démontrer la faisabilité et l’avantage d’une sélection prospective des patients en se basant sur le phénotype moléculaire des tumeurs pour orienter le choix du traitement de 1ère ligne dans le carcinome rénal à cellulaires claires métastatique et ouvre la voie à de nouveaux essais cliniques de plus grande envergure basées sur l’utilisation de biomarqueurs.
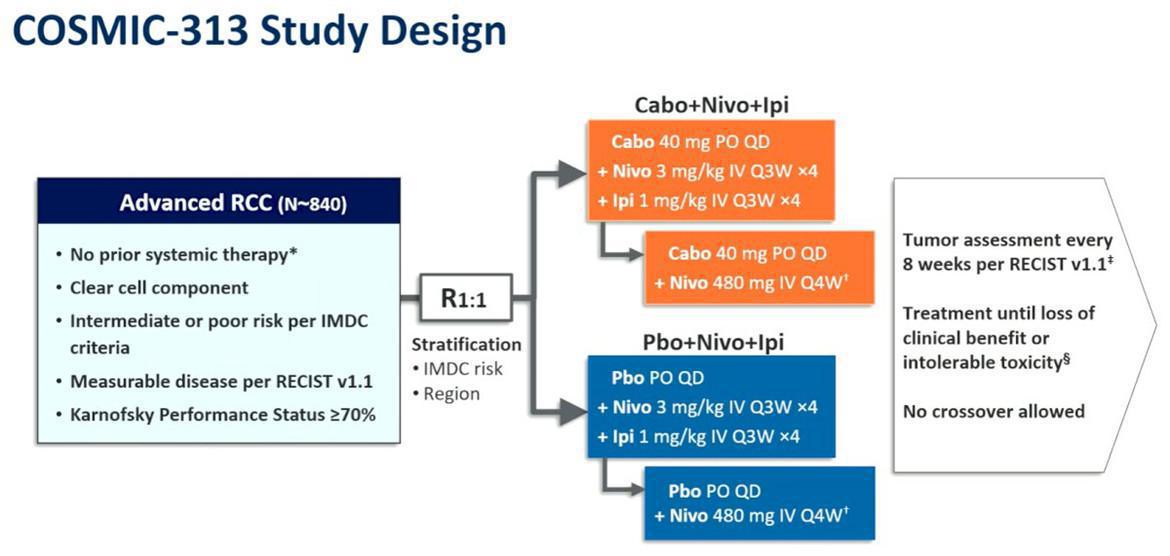
Suite à ces dernières avancées, la recherche explore de nouvelles approches pour continuer à faire progresser la prise en charge des patients atteints d’un cancer du rein métastatique. Parmi les présentations attendues à l’ESMO 2022 figuraient les premières données de l’essai de phase 3 COSMIC-313 qui évaluait pour la 1ère fois l’efficacité et la tolérance d’une combinaison de référence (Nivolumab et Ipilimumab) face à un triplet avec Cabozantinib à la dose de 40 mg/j chez les patients atteints d’un carcinome à cellules claires de pronostic intermédiaire ou défavorable.
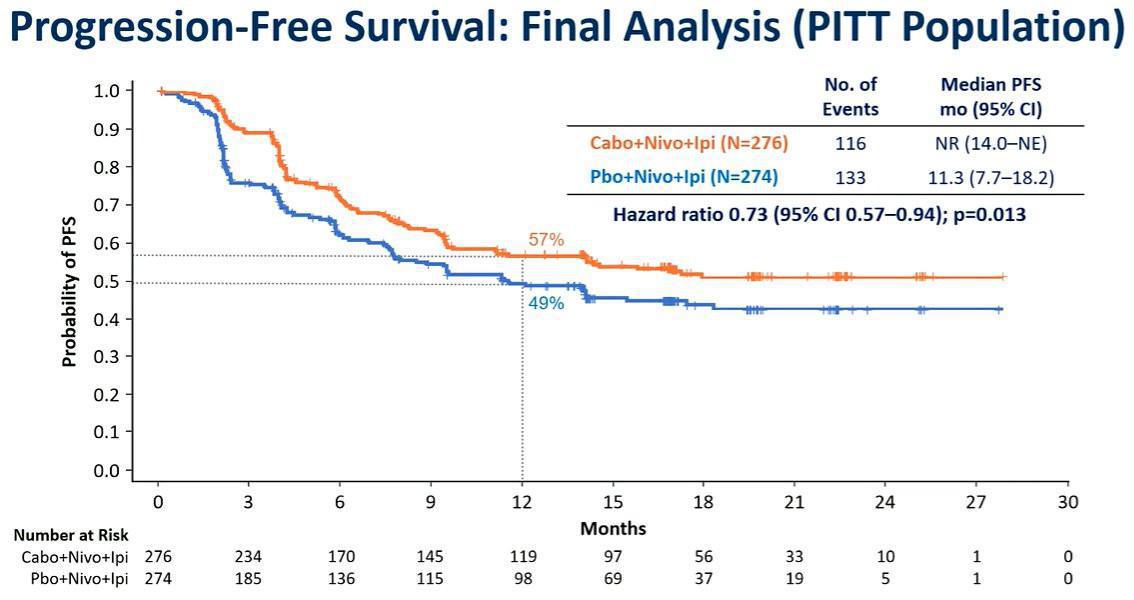
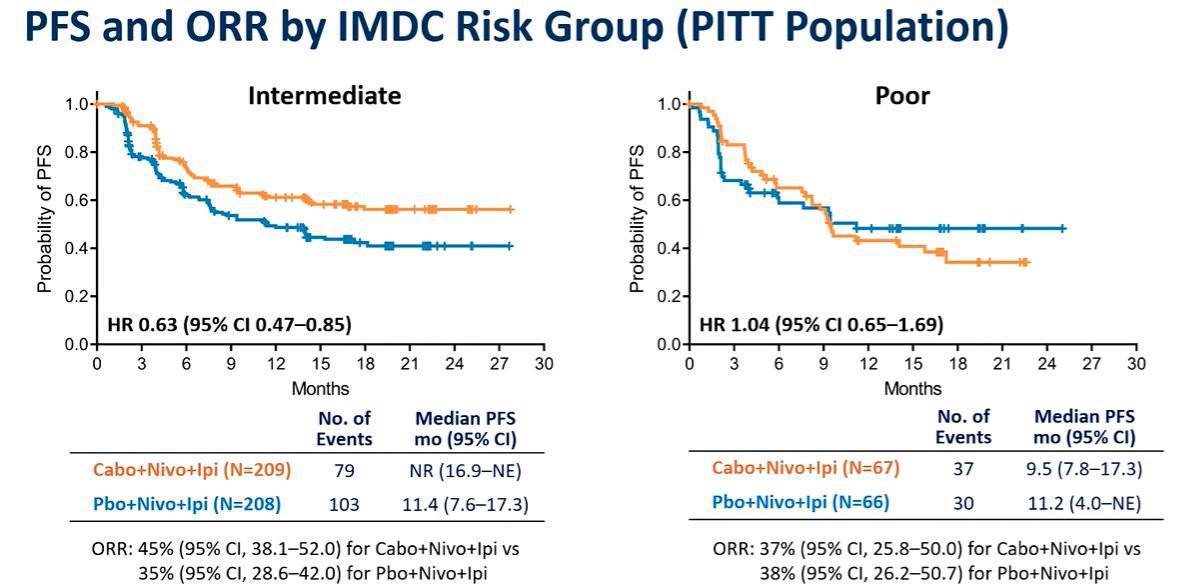
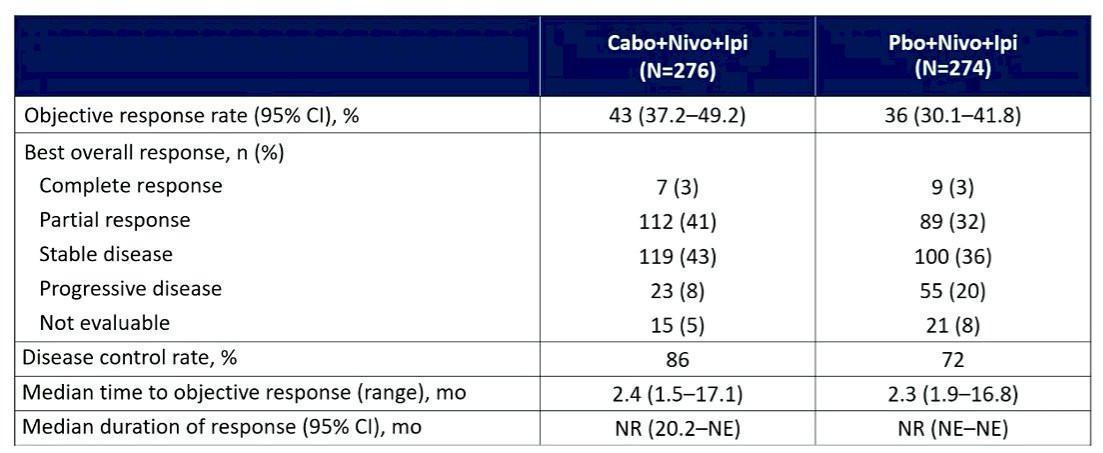
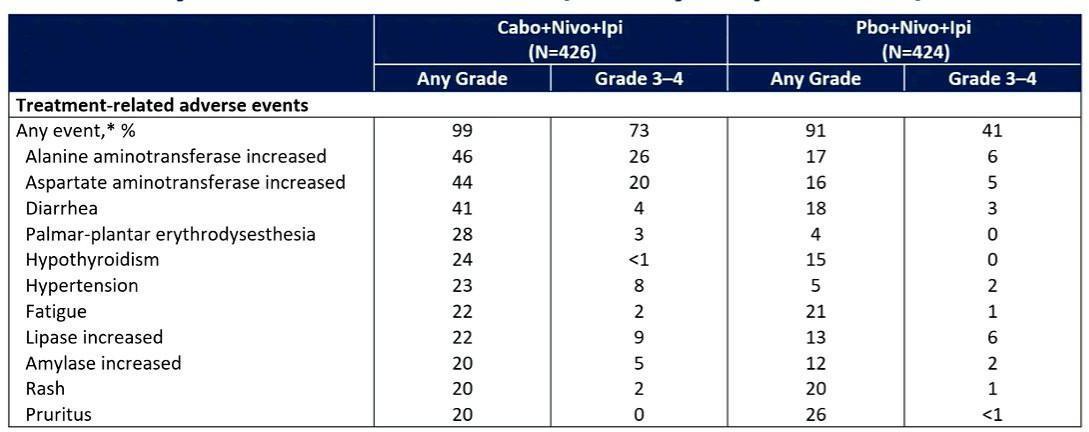
Dans cette étude, on notait une amélioration significative de la survie sans progression en faveur du triplet avec une médiane de PFS non atteinte (IC95% 14,0 mois-NE) contre 11,3 mois avec le Nivolumab et l’Ipilimumab seul (HR=0,73 ; IC95 % 0,57-0,94 ; p= 0,013). Les patients avec une maladie à risque intermédiaire semblaient bénéficier encore plus de l’ajout de Cabozantinib (HR=0,37 ; IC95%, 0,47-0,85). Les données de survie globale sont toujours en attente. Le taux de réponse objective pour le triplet était de 43 % (IC95 %, 37,2 %-49,2 %) contre 36 % (IC95 %, 30,1 %-41,8 %). Concernant le profil de tolérance, les effets indésirables étaient plus fréquents avec le Cabozantinib mais ils étaient considérés comme gérables avec toutefois 73% de grade ≥ 3 pour la triple association contre 43%.
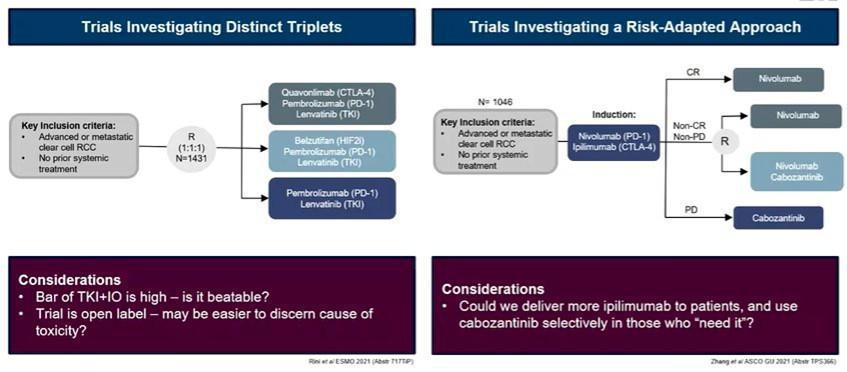
En l’absence de données de survie globale, il est difficile de prédire quelle place potentielle pourra occuper cette combinaison de 2 immunothérapies et d’un inhibiteur de tyrosine dans le paysage thérapeutique actuel du cancer du rein métastatique. En dépit d’une amélioration significative mais encore immature de la survie sans progressive, il n’existe qu’une augmentation marginale du taux de réponse objective par rapport au traitement de référence avec un faible taux de réponse complète dans les deux bras. Cette stratégie pourra peut-être être proposée à une population sélectionnée notamment en cas de maladie très agressive mais avec un profil de tolérance qui ne sera pas anodin en regard de la toxicité observée et l’effet potentiel sur la qualité de vie de ces patients. Une approche adaptative (étude PDIGREE) basée sur la réponse d’une combinaison d’immunothérapie avant l’ajout éventuelle de Cabozantinib parait peut-être plus pertinente qu’une addition de thérapies d’emblée. Plusieurs études sont en cours avec des triplets intégrant d’autres immunothérapies (anti-LAG3, anti TIGIT) ou d’autres molécules comme les inhibiteurs de HIF-2α (Belzutifan).